Ariad Pharmaceuticals-Neu
http://ih.advfn.com/p.php?pid=nmona&article=71068874
Datum: 2016.04.11 @ 7.35
Quelle : Business Wire
Lager: Ariad Pharmaceuticals, Inc. (MM) (ARIA)
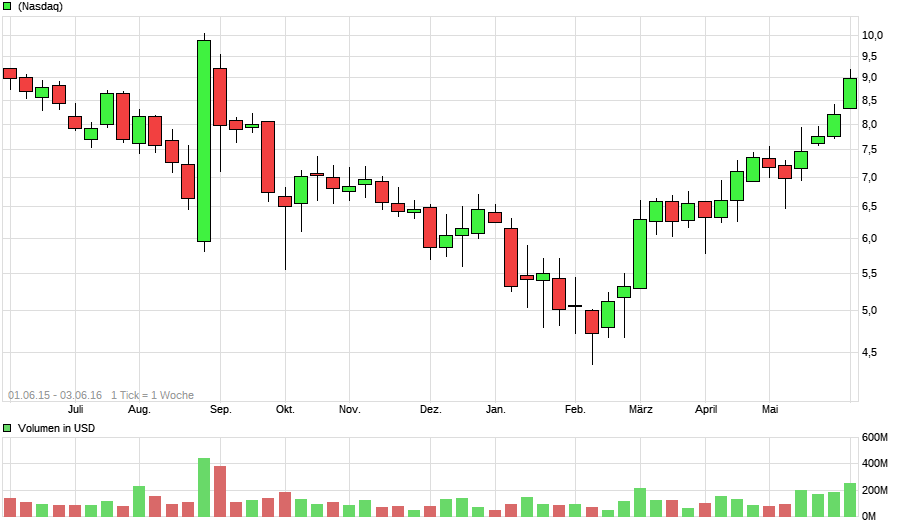
Zitat: 6.34 -0.26 (-3.94%) @ 6.21
ARIAD Pharmaceuticals, Inc. (NASDAQ: ARIA) gab heute die Einleitung einer randomisierten, First-Line-klinischen Phase-3-Studie mit brigatinib, seine Prüfpräparate anaplastischen Lymphom-Kinase (ALK) Inhibitor, bei erwachsenen Patienten mit ALK-positivem, lokal fortgeschrittenem oder metastasiertem nicht -small kleinzelligem Lungenkrebs (NSCLC), die zuvor noch nicht mit einem ALK-Inhibitor behandelt worden. Die ALTA 1L (A LK in L Ung Krebs T rial von Brig A tinib in 1. L in) Studie entwickelt, um die Wirksamkeit von brigatinib im Vergleich zu beurteilen , basierend auf der Auswertung des primären Endpunkt des progressionsfreie Überleben (PFS) auf crizotinib.
"Wir freuen uns brigatinib in eine entscheidende Phase-3-Studie als potenzielle neue Therapie werden vorrückenden für Patienten mit ALK + NSCLC, die noch nicht ein ALK-Inhibitor erhalten", sagte Tim Clackson, Ph.D., President für Forschung und Entwicklung und Chief wissenschaftlicher Mitarbeiter von ARIAD. "Wir glauben, dass die positiven Ergebnisse in unserer präklinischen und laufenden Phase gezeigt 1/2 Studien legen nahe, brigatinib das Potenzial hat, die Ergebnisse für ALK + NSCLC-Patienten auf die Behandlung mit crizotinib im Vergleich zu verbessern."
Studiendesign
Die ALTA 1L-Studie ist eine randomisierte, open-label, multizentrische, internationale Studie, die entworfen wird, um die Wirksamkeit und Sicherheit von brigatinib zu vergleichen bei erwachsenen Patienten mit ALK + NSCLC crizotinib, die nicht zuvor ein ALK-Inhibitor erhalten. Die Studie wird voraussichtlich bei etwa 150 Prüfzentren in Nordamerika, Europa und dem asiatisch-pazifischen Raum durchgeführt werden. Die Patienten in der Studie muss mindestens 18 Jahre alt sind, haben im Stadium IIIB oder IV NSCLC mit ALK-Umlagerung sein, haben nicht mehr als eine Therapie mit systemischen Krebstherapie im lokal fortgeschrittenen oder metastasierten Einstellung empfangen haben und sich nicht vor der Therapie mit ein ALK-Inhibitor.
Etwa 270 Patienten werden voraussichtlich randomisiert werden eins-zu-eins erhalten brigatinib (90 mg einmal täglich oral für sieben Tage, gefolgt von Eskalation bis 180 mg einmal täglich) oder crizotinib (250 mg zweimal täglich oral gegeben). ARIAD erwartet im Jahr 2018 die Aufnahme von Patienten in der ALTA 1L-Studie abzuschließen.
Der primäre Endpunkt der Studie ist das progressionsfreie Überleben (PFS), pro RECIST-Kriterien, wie durch einen unabhängigen, verblindeten Prüfungsausschuss (BIRC) bewertet. Ansprechen des Tumors Abschätzungen werden alle acht Wochen durchgeführt werden. Key sekundären Endpunkte umfassen die objektive Ansprechrate (ORR), intrakranielle ORR, intrakranielle PFS, die Dauer des Ansprechens, das Gesamtüberleben (OS), die Sicherheit und Verträglichkeit. Gesundheitsbezogene Lebensqualität Daten werden auch bewertet werden.
"Dieser Kopf-an-Kopf-Studie wird direkt testen brigatinib gegen crizotinib in der TKI-naiven ALK + Einstellung - wo innovative Therapien erforderlich sind, um Responseraten zu verbessern und das Fortschreiten zu verzögern, die durch die Entstehung von sekundären Resistenzmutationen in ALK und Progression auftreten kann das zentrale Nervensystem ", sagte D. Ross Camidge, MD, Ph.D., Direktor der Thoraxonkologie an der Universität von Colorado. "Bei Patienten, die crizotinib Ausfall erlebt haben, hat brigatinib schon sehr beeindruckend progressionsfreie Überleben und ausgeprägte Wirksamkeit bei Patienten mit ZNS-Metastasen zeigten - Eigenschaften, die in der ALK TKI-naive Einstellung legen nahe, dass, könnte es möglicherweise Naturgeschichte durch eine bessere Unterdrückung der Patienten ändern ALK + Krankheit von Anfang an. "
Über Brigatinib
Brigatinib ist ein Prüfpräparat, gezielte Krebsmedizin intern bei ARIAD Pharmaceuticals entdeckt, Inc. Es ist in der Entwicklung für die Behandlung von Patienten mit ALK + NSCLC. Brigatinib erhielt Durchbruch Therapie Bezeichnung von der FDA im Oktober 2014 für die Behandlung von Patienten mit ALK + NSCLC, deren Tumoren resistent sind auf der Grundlage einer laufenden Phase-1/2-Studie zu crizotinib. Brigatinib wird derzeit in der globalen Phase-2-Studie bei ALTA ALK + NSCLC-Patienten ausgewertet, die auf crizotinib Fortschritte gemacht haben, die für die Einreichung im Jahr 2016 später geplant erwartet wird, für ein neues Medikament Anwendung die Basis zu bilden.
Über ARIAD
ARIAD Pharmaceuticals, Inc., mit Hauptsitz in Cambridge, Massachusetts und Lausanne, Schweiz, ist ein Unternehmen für seltene Leiden Onkologie konzentriert sich auf das Leben von Krebspatienten mit Durchbruch Medikamente verwandeln. ARIAD auf neue Medikamente arbeiten, um die Behandlung verschiedener Formen von chronischen und akuten Leukämie, Lungenkrebs und andere schwer zu behandelnde Krebsarten Waise zu fördern. ARIAD verwendet Rechen- und strukturelle Ansätze kleinmolekularer Medikamente zu entwickeln, die Resistenz gegen vorhandene Krebsmedikamente zu überwinden. Weitere Informationen finden Sie unter http://www.ariad.com oder folgen Sie ARIAD auf Twitter (@ARIADPharm).
Vorausschauende Aussagen
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen, von denen jede in ihrer Gesamtheit durch diese vorbehaltlichen Aussagen qualifiziert sind. Alle hierin enthaltenen Aussagen, beschreiben keine historischen Tatsachen darstellen, einschließlich, aber nicht beschränkt auf, Aussagen in Bezug auf: unsere Pläne für die ALTA IL-Studie, die Studiendesign und der erwartete Zeitpunkt für den Abschluss der Einschreibung; und die Aussagen von Drs. Clackson und Camidge, sind zukunftsgerichtete Aussagen, die auf den Erwartungen des Managements basieren und unterliegen bestimmten Faktoren, Risiken und Unsicherheiten, die dazu führen können, Ausgang von Ereignissen, Timing und Leistung unterscheiden sich wesentlich von den in diesen Aussagen ausgedrückt oder impliziert werden. Zu diesen Faktoren, Risiken und Unsicherheiten beinhalten, sind aber nicht beschränkt auf, unsere laufenden strategischen Überprüfung, unsere Fähigkeit, erfolgreich zu vermarkten und generieren Gewinne aus dem Verkauf von Iclusig und unserer Produktkandidaten, wenn genehmigt; Konkurrenz von alternativen Therapien; unsere Fähigkeit, erwartete klinische Studie Beginn, Einschreibung und Fertigstellungstermine und die regulative Einreichung Termine für unsere Produkte und Produktkandidaten zu treffen und neue Entwicklungskandidaten in die Klinik zu bewegen; unsere Fähigkeit, auf unsere wichtigsten Unternehmensinitiativen auszuführen; regulatorische Entwicklungen und Sicherheitsfragen, einschließlich Schwierigkeiten oder Verzögerungen bei der Erlangung der behördlichen und Preis- und Erstattungs Zulassungen unserer Produkte auf den Markt; unser Vertrauen auf die Leistung von Drittherstellern und Spezial Apotheken für die Lieferung und den Vertrieb unserer Produkte und Produktkandidaten; das Auftreten ungünstiger Sicherheitsereignisse mit unseren Produkten und Produktkandidaten; die Kosten im Zusammenhang mit Forschung, Entwicklung, Herstellung, Vermarktung und andere Aktivitäten; das Verhalten, das Timing und die Ergebnisse der vorklinischen und klinischen Studien unserer Produkte und Produktkandidaten, einschließlich der präklinischen Daten und frühen klinischen Daten können später nicht mehr Phase der klinischen Studien repliziert werden; die Angemessenheit unserer Kapitalressourcen und die Verfügbarkeit von zusätzlichen Mittel; die Fähigkeit, unsere vertraglichen Verpflichtungen zu erfüllen, im Rahmen unserer Leasingverträge, Wandelanleihen und Lizenzfinanzierungsvereinbarungen einschließlich; Patentschutz und Dritter an geistigem Eigentum Ansprüche; Rechtsstreitigkeiten; unsere Aktivitäten im Ausland; Risiken in Bezug auf wichtige Mitarbeiter, Märkte, Wirtschaftsbedingungen, Gesundheitsreform, Preise und Erstattungssätze; und andere Risikofaktoren in unseren öffentlichen Einreichungen bei der US Securities and Exchange Commission detailliert, einschließlich unseres aktuellen Jahresbericht auf Formular 10-K und nachfolgenden Quartalsberichten auf Formular 10-Q. Sofern nicht anders angegeben, diese vorausschauenden Aussagen gelten nur ab dem Datum dieser Pressemitteilung und wir übernehmen keine Verpflichtung zur Aktualisierung oder eine dieser Aussagen zu revidieren, um Ereignisse oder Umstände, die nach dieser Pressemitteilung widerspiegeln. Wir warnen Investoren erhebliche Abhängigkeit von den zukunftsgerichteten Aussagen in dieser Pressemitteilung zu verlassen.
Quelltext anzeigen Version auf businesswire.com: http://www.businesswire.com/news/home/20160411005072/en/
ARIAD Pharmaceuticals, Inc.
Für Investoren
Maria Cantor, (617) 621-2208
Maria.Cantor@ariad.com
oder
Für Medien
Liza heapes, (617) 621-2315
Liza.Heapes@ariad.com
GENEVA & CAMBRIDGE, Mass.--(BUSINESS WIRE)--Apr. 15, 2016
http://investor.ariad.com/...p=RssLanding&cat=news&id=2157495
http://investor.ariad.com/...22&p=irol-newsArticle&ID=2158206
Die erste Präsentation von vorklinischen Daten Unterstützt nächsten Klinische Tests in nicht-kleinzelligem Lungenkrebs-Patienten mit EGFR und HER2 Exon 20 Mutationen
CAMBRIDGE, Mass. & NEW ORLEANS - (BUSINESS WIRE) - April 19, 2016-- ARIAD Pharmaceuticals, Inc. (NASDAQ: ARIA) gab heute die Ergebnisse einer umfassenden präklinischen Studien auf seine Prüfpräparate Tyrosinkinase-Inhibitor (TKI), AP32788, bei der American Association for Cancer Research (AACR) Annual Meeting 2016. AP32788 ein TKI ist entworfen, um spezifische Mutationen in EGFR oder HER2 in einer Untergruppe von Patienten mit nicht-kleinzelligem Lungenkrebs (NSCLC) zum Ziel, für den gibt es noch keine gezielten Therapien zur Verfügung. Die Phase 1/2 der klinischen Prüfung AP32788 wird voraussichtlich im zweiten Quartal 2016 die Aufnahme von Patienten zu beginnen.
Die präsentierten Daten wurden in einer mündlichen Präsentation enthalten Titel "AP32788, ein potenter, selektiver Inhibitor von EGFR und HER2 onkogenen Mutanten, einschließlich Exon 20 Einschübe, in präklinischen Modellen." Die Forschung von ARIAD Wissenschaftler zeigte, dass in einem aufeinander abgestimmten Satz von technischen Zelllinien gehemmt AP32788 alle getesteten EGFR und HER2-Mutanten, einschließlich Exon 20 Insertionsmutanten mit Selektivität gegenüber dem Wildtyp (WT) EGFR. Hemmung der WT EGFR in Nicht-Tumorzellen wurde mit Dosis-limitierenden Toxizitäten von EGFR-Inhibitoren bei Patienten in Verbindung gebracht. Enzymatische Analyse bestätigte, dass AP32788 irreversibel inaktiviert EGFR Exon 20 mit 20fache Selektivität gegenüber WT EGFR, im Gegensatz zu den anderen getesteten EGFR-TKI. AP32788 auch Tumor-Regressionen in einem Maus-EGFR Exon 20 Modell bei Dosen induziert, die gut vertragen wurden.
"Diese präklinischen Daten auf AP32788 sein Potenzial zeigen zu potent Exon 20 mutierte Formen von EGFR und HER2 hemmen, die von derzeit verfügbaren TKI Behandlungen nicht angesprochen werden", sagte Timothy P. Clackson , Ph.D., President für Forschung und Entwicklung und Chief Scientific Officer bei ARIAD. "Die Selektivität Daten deuten darauf hin, dass wirksame Spiegel der Exposition gegenüber AP32788 bei Patienten mit diesen herausfordernden Mutationen erreichbar sein kann -a Hypothese, die wir in der Phase 1/2 Studie testen wird. Wir glauben, AP32788 die erste TKI ist, die die zugrunde liegende Mutation zu hemmen, die in diesen orphan onkologischen Krankheit Subsets entwickelt und optimiert wurde. "
Über nicht-kleinzelligem Lungenkrebs, EGFR und HER2
Nicht-kleinzelliger Lungenkrebs (NSCLC) ist die häufigste Form von Lungenkrebs, für etwa 85 Prozent der geschätzten 221.200 neue Fälle von Lungenkrebs im Jahr 2015 diagnostiziert Buchhaltung in der Die Vereinigten Staaten , entsprechend der American Cancer Society . EGFR-Mutationen stellen die größte bekannte, anzielbare Teilmenge von NSCLC. Während die häufigsten Arten von EGFR - Mutation von zugelassenen TKI - Therapien behandelt werden, gibt es keine Möglichkeiten der Behandlung gezielt für die etwa 4 bis 9 Prozent der EGFR-mutierten Tumoren der Lunge mit Exon 20 Insertionsmutationen 1. Außerdem können Patienten mit HER2 - Mutationen, meist Exon 20 Insertionsmutationen umfassen etwa 2 Prozent der NSCLC - Patienten 2 und haben auch keine aktuellen Behandlungsmöglichkeiten. ARIAD schätzt, dass es etwa 6.000 Patienten in Die Vereinigten Staaten Leben mit EGFR Exon 20 oder HER2 Punktmutationen, basierend auf den verfügbaren Daten ab 2014 die Anzahl der Stufe IIIB oder IV NSCLC und dem geschätzten Prozentsatz der Patienten mit diesen Mutationen.
Über AP32788
AP32788 ist ein Prüfpräparat orale Tyrosinkinase-Inhibitor (TKI) von Mutationen in EGFR und HER2 aktivieren. Das Molekül wurde entwickelt, um die ungedeckten Bedarf bei Patienten mit nicht-kleinzelligem Lungenkrebs (NSCLC), angetrieben durch Exon 20 Insertion Mutationen in EGFR und HER2 zu adressieren, und ist vierte intern entdeckt Onkologie IND des ARIAD für die klinische Entwicklung geräumt werden.
Über ARIAD
ARIAD Pharmaceuticals, Inc. Mit Sitz in Cambridge, Massachusetts und Lausanne, Schweiz Ist eine Waise Onkologie-Unternehmen konzentriert sich auf das Leben von Krebspatienten mit Durchbruch Medikamente verwandeln. ARIAD auf neue Medikamente arbeiten, um die Behandlung verschiedener Formen von chronischen und akuten Leukämie, Lungenkrebs und andere schwer zu behandelnde Krebsarten Waise zu fördern. ARIAD verwendet Rechen- und strukturelle Ansätze kleinmolekularer Medikamente zu entwickeln, die Resistenz gegen vorhandene Krebsmedikamente zu überwinden. Weitere Informationen finden Sie unter http://www.ariad.com oder folgen Sie ARIAD auf Twitter ( @ARIADPharm ).
Vorausschauende Aussagen
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen, von denen jede in ihrer Gesamtheit durch diese vorbehaltlichen Aussagen qualifiziert sind. Alle hierin enthaltenen Aussagen, die beschreiben keine historischen Tatsachen darstellen, einschließlich, aber nicht beschränkt auf unsere Aussagen über den Zeitpunkt der erwarteten Patientenrekrutierung in der Phase 1/2 der klinischen Prüfung AP32788 und der Erklärungen von Dr. Clackson beschränkt, sind zukunftsgerichtete Aussagen , die auf den Erwartungen des Managements und unterliegen bestimmten Faktoren, Risiken und Unsicherheiten, welche die tatsächlichen Ergebnisse, die Ergebnisse der Ereignisse, Timing und Leistungen erheblich von denen verursachen können in diesen Aussagen ausgedrückt oder impliziert werden. Zu diesen Faktoren, Risiken und Unsicherheiten beinhalten, sind aber nicht beschränkt auf, unsere laufenden strategischen Überprüfung, unsere Fähigkeit, erfolgreich zu vermarkten und generieren Gewinne aus dem Verkauf von Iclusig und unserer Produktkandidaten, wenn genehmigt; Konkurrenz von alternativen Therapien; unsere Fähigkeit, erwartete klinische Studie Beginn, Einschreibung und Fertigstellungstermine und die regulative Einreichung Termine für unsere Produkte und Produktkandidaten zu treffen und neue Entwicklungskandidaten in die Klinik zu bewegen; unsere Fähigkeit, auf unsere wichtigsten Unternehmensinitiativen auszuführen; regulatorische Entwicklungen und Sicherheitsfragen, einschließlich Schwierigkeiten oder Verzögerungen bei der Erlangung der behördlichen und Preis- und Erstattungs Zulassungen unserer Produkte auf den Markt; unser Vertrauen auf die Leistung von Drittherstellern und Spezial Apotheken für die Lieferung und den Vertrieb unserer Produkte und Produktkandidaten; das Auftreten ungünstiger Sicherheitsereignisse mit unseren Produkten und Produktkandidaten; die Kosten im Zusammenhang mit Forschung, Entwicklung, Herstellung, Vermarktung und andere Aktivitäten; das Verhalten, das Timing und die Ergebnisse der vorklinischen und klinischen Studien unserer Produkte und Produktkandidaten, einschließlich der präklinischen Daten und frühen klinischen Daten können später nicht mehr Phase der klinischen Studien repliziert werden; die Angemessenheit unserer Kapitalressourcen und die Verfügbarkeit von zusätzlichen Mittel; die Fähigkeit, unsere vertraglichen Verpflichtungen zu erfüllen, im Rahmen unserer Leasingverträge, Wandelanleihen und Lizenzfinanzierungsvereinbarungen einschließlich; Patentschutz und Dritter an geistigem Eigentum Ansprüche; Rechtsstreitigkeiten; unsere Aktivitäten im Ausland; Risiken in Bezug auf wichtige Mitarbeiter, Märkte, Wirtschaftsbedingungen, Gesundheitsreform, Preise und Erstattungssätze; und andere Risikofaktoren in unseren öffentlichen Einreichungen bei der detaillierten US Securities and Exchange Commission , Unserem jüngsten Jahresbericht auf Formblatt 10-K und nachfolgenden Quartalsberichten auf Formular 10-Q einschließlich. Sofern nicht anders angegeben, diese vorausschauenden Aussagen gelten nur ab dem Datum dieser Pressemitteilung und wir übernehmen keine Verpflichtung zur Aktualisierung oder eine dieser Aussagen zu revidieren, um Ereignisse oder Umstände, die nach dieser Pressemitteilung widerspiegeln. Wir warnen Investoren erhebliche Abhängigkeit von den zukunftsgerichteten Aussagen in dieser Pressemitteilung zu verlassen.
1 Costa, D. 2015. EGFR Exon 20 Insertion in nicht-kleinzelligem Lungenkrebs. Mein Krebs Genome http://www.mycancergenome.org/content/disease/...ancer/egfr/64/http:/ / www.mycancergenome.org/content/disease/lung-cancer/egfr/64/ (Updated 5. November 2015 ).
2 JCO 22, April 2013 JCO.2012.45.6095
Quelltext anzeigen Version auf businesswire.com: http://www.businesswire.com/news/home/20160419005162/en/
Quelle: ARIAD Pharmaceuticals, Inc.
ARIAD Pharmaceuticals, Inc.
Für Investoren
Maria Cantor, 617-621-2208
Maria.cantor@ariad.com
oder
Für Medien
Liza heapes, 617-621-2315
Liza.heapes@ariad.com
http://ih.advfn.com/p.php?pid=nmona&article=71249821
ARIAD to Webcast Conference Call on First Quarter 2016 Financial Results
Date : 04/26/2016 @ 7:35AM
Source : Business Wire
Stock : Ariad Pharmaceuticals, Inc. (MM) (ARIA)
Quote : 7.25 -0.11 (-1.49%) @ 8:00PM
ARIAD Pharmaceuticals, Inc. (NASDAQ: ARIA) gab heute bekannt, dass es seine erste Quartal 2016 Finanzergebnisse am Dienstag, 10. Mai 2016 Bericht erstatten wird, bevor der Markt öffnet. Nach der Ankündigung, um 8:30 Uhr Eastern Time, wird Unternehmensleitung eine Telefonkonferenz und Webcast Diskussion der Ergebnisse veranstalten und eine allgemeine Unternehmens-Update zur Verfügung stellen.
Der Live-Webcast kann auf http://investor.ariad.com durch den Besuch der Investor Relations-Seite der Website des Unternehmens abgerufen werden. Der Anruf kann unter der Rufnummer 888 erreichbar 311-8173 (Inland) oder 330-863-3376 (international) 5 Minuten vor der Startzeit und die Bereitstellung der Passcode 84030796. Eine Aufzeichnung der Telefonkonferenz wird etwa auf der ARIAD Website zur Verfügung stehen 2 Stunden nach dem Aufruf Fertigstellung und wird drei Wochen lang archiviert werden.
Über ARIAD
ARIAD Pharmaceuticals, Inc., mit Hauptsitz in Cambridge, Massachusetts und Lausanne, Schweiz, ist ein Unternehmen für seltene Leiden Onkologie konzentriert sich auf das Leben von Krebspatienten mit Durchbruch Medikamente verwandeln. ARIAD auf neue Medikamente arbeiten, um die Behandlung verschiedener Formen von chronischen und akuten Leukämie, Lungenkrebs und andere schwer zu behandelnde Krebsarten Waise zu fördern. ARIAD verwendet Rechen- und strukturelle Ansätze kleinmolekularer Medikamente zu entwickeln, die Resistenz gegen vorhandene Krebsmedikamente zu überwinden. Weitere Informationen finden Sie unter http://www.ariad.com oder folgen Sie ARIAD auf Twitter (@ARIADPharm).
Quelltext anzeigen Version auf businesswire.com: http://www.businesswire.com/news/home/20160426005157/en/
ARIAD Pharmaceuticals, Inc.
Für Investoren
Maria Cantor, 617-621-2208
Maria.cantor@ariad.com
oder
Für Medien
Liza heapes, 617-621-2315
Liza.heapes@ariad.com
http://phx.corporate-ir.net/...ZT0z&t=1&cb=635938284881264087
http://services.corporate-ir.net/SEC.Enhanced/...422&fid=14359966
9-Mai-2016
Der Eintritt in einen Werkstoff endgültige Vereinbarung, die Schaffung eines Direkt Financ
https://biz.yahoo.com/e/160509/aria8-k.html
Artikel 1.01. Der Eintritt in einen Werkstoff endgültige Vereinbarung.
Eintritt in die europäische Transaktions
Am 9. Mai 2016 ARIAD Pharmaceuticals, Inc. ( "ARIAD") und ihre hundertprozentige Tochtergesellschaft ARIAD Pharmaceuticals (Cayman) LP (die "Verkäufer") trat in einen Aktienkaufvertrag (der "Aktienkaufvertrag") mit Incyte Corporation ( "Incyte") (als Garant) und ihre hundertprozentige Tochtergesellschaft Incyte Europe Sarl ( "Incyte Europe"), gemäß denen Incyte Europa zugestimmt hat, von dem Verkäufer alle ausstehenden Aktien von ARIAD Pharmaceuticals (Luxemburg) Sarl zu erwerben , die Muttergesellschaft von ARIAD der europäischen Tochtergesellschaften verantwortlich für die Vermarktung von Iclusig® (Ponatinibs) in der Europäischen Union ( "EU") und 22 weiteren Ländern, darunter die Schweiz, Norwegen, der Türkei, Israel und Russland (das "Gebiet"), für eine Vorauszahlung in Höhe von $ 140.000.000 (die "Upfront Payment").
Im Zusammenhang mit den von der Aktienkaufvertrag vorgesehenen Transaktionen haben sich die Parteien einigten sich auch auf eine geänderte und Buy-in-Lizenzvertrag Angepasst in zwischen ARIAD, Incyte (als Bürgin) und ARIAD Pharmaceuticals (Europe) Sarl, einer der eingegeben werden Unternehmen, die von Incyte beim Schließen der vorgesehenen Transaktionen durch den Aktienkaufvertrag (die "Lizenzvereinbarung") im Besitz sein wird. Gemäß den Bedingungen der Lizenzvereinbarung wird Incyte eine exklusive Lizenz zur Entwicklung und Vermarktung Iclusig im Territorium (die "Lizenz") gewährt werden. ARIAD wird abgestufte Lizenzgebühren von Incyte zwischen 32% und 50% des Nettoumsatzes von Iclusig im Territorium (die "Lizenzgebühren") zu empfangen berechtigt. Die Lizenzgebühren für bestimmte Ereignisse Anpassung unterliegen, einschließlich dem Ablauf der gesetzlichen oder regulatorischen Ausschließlichkeitsfristen für die Vermarktung von Iclusig im Gebiet bezogene Ereignisse. Darüber hinaus wird ARIAD sein Anspruch auf $ 135.000.000 Potentialentwicklung und regulatorische Meilensteine für Iclusig in neue onkologische Indikationen in dem Gebiet erhalten auf, zusammen mit weiteren Meilensteine für nicht-onkologische Indikationen, wenn genehmigt, in dem Gebiet (zusammen die " Milestone Payments "). Incyte hat sich bereit erklärt in jedem von 2016 bis 7.000.000 $ zu leisten und 2017 ARIAD der OPTIC und OPTIC-2L klinischen Studien (die "Entwicklungskosten") zu finanzieren.
Die Bedingungen der Lizenzvereinbarung auch eine Option (die "Option") für einen Käufer von ARIAD auf die lizenzierten Rechte von Incyte, unter bestimmten Bedingungen wieder kaufen. Bei Ausübung der Option würde ARIAD des Erwerbers benötigt, um eine Zahlung zu Incyte in Höhe der Abschlagszahlung und alle Meilensteinzahlungen oder Entwicklung zu machen Kosten, die zuvor zu ARIAD bezahlt, und eine zusätzliche Zahlung basierend auf Iclusig Verkäufe in dem Gebiet, in den 12 Monaten unmittelbar vor der Ausübung der Option. Nach Ausübung der Option würde Incyte auch Anspruch auf Lizenzgebühren von durch einen Erwerber von ARIAD nach dem Tag des Inkrafttretens des Rückkaufs des Lizenz zwischen 20% bis 25% des Nettoumsatzes von Iclusig in dem Gebiet zu erhalten. Die Option kann nicht vor Ablauf des zweiten Jahres-Jubiläum ausgeübt werden oder nach dem sechs jährigen Jubiläum der Tag des Inkrafttretens der Lizenzvereinbarung. Nach Ausübung der Option ist eine weitere Übergangszeit von bis zu einem Jahr vor dem Rückkauf der Lizenz kann wirksam gemacht werden.
ARIAD und Incyte wird einen gemeinsamen Lenkungsausschuss und die gemeinsame Vermarktung Ausschuss, der Produktentwicklung und Vermarktung von Iclusig im Gebiet, einschließlich der Aufsicht über jede Entwicklung oder Kommerzialisierung Plan zu überwachen. Jeder von ARIAD und Incyte hat oberste Entscheidungskompetenz in Bezug auf eine bestimmte begrenzte Anzahl von Fragen und für alle anderen Fragen muss die Angelegenheit einvernehmlich gelöst werden oder durch ein beschleunigtes Schiedsverfahren.
Es sei denn, früher in Übereinstimmung mit dessen Bestimmungen beendet, wird die Lizenzvereinbarung in der Tat auf der Grundlage von Land zu Land weiter, bis spätestens (1) das Ablaufdatum der Zusammensetzung Patent in dem betreffenden Land zu kommen, (2) das Ablauf von einer bestimmten Aufsichts Marketing Exklusivitätsperiode oder andere gesetzliche Bezeichnung, die für die Vermarktung von Iclusig in diesem Land und (3) der siebte Jahrestag der ersten kommerziellen Verkauf von Iclusig in einem solchen Land ähnliche Exklusivität zur Verfügung stellt; und danach in Abwesenheit von Konkurrenz durch Generika, für einen bestimmten Zeitraum, in der Incyte verpflichtet, Lizenzgebühren zu zahlen, zu einem reduzierten Preis. Die Lizenz
Abkommen kann in seiner Gesamtheit durch Incyte für Bequemlichkeit auf 12 Monate feststellen, nach dem dritten Jahrestag des Wirksamkeitsdatum der Lizenz gekündigt werden. Der Lizenzvertrag kann von jeder Partei unter bestimmten anderen Umständen beendet werden, einschließlich erheblicher Verletzung, höhere Gewalt und Konkurs oder Insolvenz der anderen Partei.
Der Abschluss im Rahmen des Aktienkaufvertrag und Wirksamkeit der Lizenzvereinbarung wird zur Zeit am oder um den 1. Juni erwartet wird, 2016, vorbehaltlich der Erfüllung der üblichen Abschlussbedingungen. Der Aktienkaufvertrag ist nicht auf Incyte die Fähigkeit Europas, bedingt Finanzierung zu erhalten. Darüber hinaus enthält der Aktienkaufvertrag zum Stillstand Bestimmung, dass Incyte schließt aus mehr als einen bestimmten Prozentsatz der Aktien von ARIAD Stammaktien oder von der Einnahme bestimmter anderer Maßnahmen beabsichtigt den Erwerb der Zustimmung von ARIAD des Board of Directors zu erwerben oder zu beeinflussen Kontrolle von ARIAD ohne eine bestimmte Zeit nach dem Datum des Inkrafttretens der Vereinbarung, vorbehaltlich bestimmter Ausnahmen üblich.
Die vorstehenden Beschreibungen der Aktienkaufvertrag und den Lizenzvertrag erheben keinen Anspruch auf Vollständigkeit und sind in ihrer Gesamtheit durch Bezugnahme auf die volle Vereinbarungen qualifiziert, die ARIAD als Exponate in seinem Quartalsbericht auf Formular 10-Q für das Quartal einzureichen beabsichtigt zum 30. Juni 2016. Eine Kopie der Pressemitteilung die Transaktionen hierin beschriebenen Ankündigung auf dem Formular zu diesem aktuellen Bericht beigefügt ist 8-K als Anlage 99.1 und wird hierin durch Bezugnahme aufgenommen.
Geänderte Lizenz Finanzierung
Am 28. Juli 2015 trat ARIAD in eine Revenue Interest Abtretungsvertrag (die "RIAA") mit PDL BioPharma, Inc. ( "PDL"). Unter der RIAA, stimmte PDL ARIAD 100.000.000 $ für das Recht zahlen, um einen mittleren einstelligen einstelligen Prozent der weltweiten Nettoumsatz aus dem Verkauf von Iclusig erhalten, bis sie eine feste interne Rendite erhält. Darüber hinaus erhielt ARIAD eine Option PDL zu verlangen, eine zusätzliche $ 100 Millionen entweder eine oder zwei Tranchen von Januar bis Juli 2016 ARIAD bis zu finanzieren.
Am 9. Mai 2016 im Zusammenhang mit den Transaktionen mit Incyte oben beschrieben, ARIAD und PDL bereit erklärt, die RIAA an, unter anderem sind in der Iclusig Nettoumsatz Berechnung unter den RIAA einen Nettoumsatz von Iclusig gemacht von Incyte in dem Gebiet zu ändern unter der Lizenzvereinbarung. Darüber hinaus nach Wahl des ARIAD zusätzliche Mittel erhalten wurde so umstrukturiert, dass ARIAD kann PDL erfordern eine zusätzliche $ 40 Mio. (statt der ursprünglichen $ 100.000.000) im Juli 2017 (statt zwischen Januar und Juli 2016) zur Finanzierung auf. Im Zusammenhang mit der Änderung der RIAA, ARIAD und PDL auch vereinbart, ARIAD die europäischen Patente und bestimmten anderen europäischen Vermögenswerte aus der Sicherheiten freizugeben. Diese Vereinbarungen mit PDL unterliegen und wirksam bei der Schließung der Incyte Transaktion.
Die vorstehende Zusammenfassung der Änderung der RIAA und der Veröffentlichung von Sicherheitsinteressen erhebt nicht den Anspruch auf Vollständigkeit und ist in seiner Gesamtheit durch Bezugnahme auf die volle Vereinbarungen qualifiziert, die ARIAD als Exponate in seinem Quartalsbericht einzureichen beabsichtigt, auf dem Formular 10-Q für das Quartal bis 30. Juni 2016.
Mit Ausnahme ihres Status als Vertragsunterlagen zwischen den Parteien, dem Aktienkaufvertrag, Lizenzvertrag, und Änderungen der RIAA und Sicherungsvertrag nicht sachliche Informationen über die jeweiligen Parteien liefern soll. Die Darstellungen und in jeder dieser Vereinbarungen enthaltenen Garantien wurden nur zum Zwecke eines jeden solchen Vereinbarung und wie der dort festgelegten Zeitpunkt gemacht, waren ausschließlich zum Nutzen der jeweiligen Parteien auf diese Vereinbarungen, und vereinbarten Beschränkungen unterliegen können durch die zu Vertragsparteien, auch durch Angaben zwischen den Parteien qualifiziert werden. Diese Zusicherungen und Gewährleistungen haben können für die Zuteilung Vertrags Risiko zwischen den Parteien der Vereinbarung zu, statt der Festlegung dieser Angelegenheiten als Tatsachen gemacht worden und kann auf Normen der Wesentlichkeit für den Vertragsparteien unterliegen, die sich von denen für Anleger unterscheiden. Dementsprechend sollten sie nicht von den Anlegern als Aussagen von Sachinformationen auf diese zu stützen.
Artikel 2.03. Schaffung einer direkten finanziellen Verpflichtung oder eine Verpflichtung aus einer Off-Bilanz Anordnung eines Registranten.
Die Angaben, die unter der Überschrift "Änderung des Lizenz Finanzierung" in Artikel 1.01 des aktuellen Bericht auf Formular 8-K wird hiermit durch Bezugnahme in diese Artikel 2.03 integriert.
Artikel 9.01 Abschluss und Exponate.
(D) Die folgenden Exponate sind mit diesem Bericht eingereicht:
Exhibit No. Beschreibung
99,1 Pressemitteilung, vom 9. Mai 2016 von ARIAD ausgegeben
Pharmaceuticals, Inc. und Incyte
Vorausschauende Aussagen
Dieses Formular 8-K enthält in die Zukunft gerichtete Aussagen, von denen jede in ihrer Gesamtheit durch diese vorbehaltlichen Aussagen qualifiziert sind. Alle hierin enthaltenen Aussagen, beschreiben keine historischen Tatsachen darstellen, einschließlich, aber nicht beschränkt auf Aussagen im Zusammenhang mit dem erwarteten Abschluss der vorgeschlagenen Transaktion mit Incyte und dem Zeitpunkt des Abschlusses der Transaktion, sind zukunftsgerichtete Aussagen, die auf den Erwartungen des Managements beruhen und unter bestimmten Faktoren, Risiken und Unsicherheiten, die aus tatsächlichen Ergebnisse, Ergebnis der Ereignisse, den Zeitpunkt und die Leistung zu unterscheiden den geäußerten oder implizierten durch solche Aussagen führen können. Zu diesen Faktoren, Risiken und Unsicherheiten beinhalten, sind aber nicht beschränkt auf, unsere laufenden strategischen Überprüfung, unsere Fähigkeit, erfolgreich zu vermarkten und generieren Gewinne aus dem Verkauf von Iclusig und unserer Produktkandidaten, wenn genehmigt; Konkurrenz von alternativen Therapien; unsere Fähigkeit, erwartete klinische Studie Beginn, Einschreibung und Fertigstellungstermine und die regulative Einreichung Termine für unsere Produkte und Produktkandidaten zu treffen und neue Entwicklungskandidaten in die Klinik zu bewegen; unsere Fähigkeit, auf unsere wichtigsten Unternehmensinitiativen auszuführen; regulatorische Entwicklungen und Sicherheitsfragen, einschließlich Schwierigkeiten oder Verzögerungen bei der Erlangung der behördlichen und Preis- und Erstattungs Zulassungen unserer Produkte auf den Markt; unser Vertrauen auf die Leistung von Drittherstellern und Spezial Apotheken für die Lieferung und den Vertrieb unserer Produkte und Produktkandidaten; das Auftreten ungünstiger Sicherheitsereignisse mit unseren Produkten und Produktkandidaten; die Kosten im Zusammenhang mit Forschung, Entwicklung, Herstellung, Vermarktung und andere Aktivitäten; das Verhalten, das Timing und die Ergebnisse der vorklinischen und klinischen Studien unserer Produkte und Produktkandidaten, einschließlich der präklinischen Daten und frühen klinischen Daten können später nicht mehr Phase der klinischen Studien repliziert werden; die Angemessenheit unserer Kapitalressourcen und die Verfügbarkeit von zusätzlichen Mittel; die Fähigkeit, unsere vertraglichen Verpflichtungen zu erfüllen, im Rahmen unserer Leasingverträge, Wandelanleihen und Lizenzfinanzierungsvereinbarungen einschließlich; Patentschutz und Dritter an geistigem Eigentum Ansprüche; Rechtsstreitigkeiten; unsere Aktivitäten im Ausland; Risiken in Bezug auf wichtige Mitarbeiter, Märkte, Wirtschaftsbedingungen, Gesundheitsreform, Preise und Erstattungssätze; und andere Risikofaktoren in unseren öffentlichen Einreichungen bei der US Securities and Exchange Commission detailliert, einschließlich unseres aktuellen Jahresbericht auf Formular 10-K und nachfolgenden Quartalsberichten auf Formular 10-Q. Sofern nicht anders angegeben, diese vorausschauenden Aussagen gelten nur ab dem Datum dieses Formular 8-K, und wir übernehmen keine Verpflichtung eine dieser Aussagen zu aktualisieren oder zu revidieren, um Ereignisse oder Umstände nach dem Einreichen dieser Form 8-K auftreten zu reflektieren . Wir warnen Investoren erhebliche Abhängigkeit von den zukunftsgerichteten Aussagen in dieser Form 8-K zu verlassen.
https://m.holdingschannel.com/all/...y-sarissa-capital-management-lp/
http://www.smarteranalyst.com/2016/05/18/...pharmaceuticals-inc-anac/
Cowen Analyst Chris Shibutani war mit einer Research Note auf Ariad Pharmaceuticals, Inc. (NASDAQ: ARIA ) und umreißt seine Erwartungen für die klinische Abstracts des Unternehmens für die kommenden American Society of Clinical Oncology (ASCO) 2016.
Shibutani schrieb: "Die Anleger sollten bedenken, dass die Informationen in der Zusammenfassung enthalten einen begrenzten Teil des gesamten Datensatzes darstellt, die auf der ASCO (mündliche Präsentation, Montag 6. Juni) präsentiert wird. Die Zusammenfassung wird auf Patientendaten bis Ende November, mit 3-Monate von zusätzlichen Daten (bis Ende Februar) umfassen. Wir werden uns auf PFS Daten fokussiert werden - jedoch unter Hinweis darauf, dass die PFS in der Zusammenfassung nicht voll ausgereift sein wird. Recall, die PFS aus der Phase-I / II-Daten betrug 13,4 Monate in der Zweitlinien (Patienten, die zuvor mit Crizotinib behandelt worden war). Mit PFS in der zweiten Zeile berichtet reicht von derzeit verfügbaren Medikamente einstellen, von 6-9 Monate, (rechnen wir mit einem Differential in der letzten vollständigen Datensatz von + 2-3 Monate im Vergleich zu Wettbewerber Drogen) die Auswirkungen von brigatinib eine stärkere PFS demonstrieren wäre Material auf die Einnahmemöglichkeiten, sowohl in Bezug auf Aktien sowie längere Dauer der Patienten auf das Medikament zu bleiben. "
Shibutani wiederholte ein Outperform-Rating auf Aktien von Ariad, mit einem Kursziel von $ 10, die eine auf den Kopf von 28% vom aktuellen Niveau impliziert.
Nach TipRanks.com , die Erfolgsrate der Analysten und Blogger misst basierend darauf , wie ihre Anrufe durchführen, hat Analyst Chris Shibutani eine jährliche durchschnittliche Rendite von 1,3% und eine 40% Erfolgsquote. Shibutani hat einen 11,1% durchschnittliche Rendite bei ARIA zu empfehlen, und ist auf Platz # 2156 von 3910 Analysten rangiert.
Von den fünf Analysten von TipRanks abgefragt (in den letzten 3 Monate), 3 Rate Ariad Lager ein Kauf, 1 Raten die Aktie ein Halten und 1 empfiehlt einen Verkauf. Mit einem Ertragspotenzial von 24,5%, der Konsensus-Kursziel der Aktie beläuft sich auf 9,60 $.
http://finance.yahoo.com/news/...reimbursement-iclusig-113500648.html
CAMBRIDGE, Mass .-- (BUSINESS WIRE) -
ARIAD Pharmaceuticals, Inc. ( ARIA ) gab heute bekannt , dass die Verhandlungen mit dem Wirtschaftsausschuss für Gesundheitspflege - Produkte in Frankreich in Bezug auf Preisgestaltung und Erstattung für Iclusig ® (Ponatinibs) haben nun abgeschlossen. Als Ergebnis wird ARIAD Nettoproduktumsatz auf kumulative Sendungen in Frankreich von etwa $ 25 Mio. im zweiten Quartal 2016 im Zusammenhang mit aufzunehmen.
Iclusig hat sich seit Ende 2012 durch eine vorlizenziert Vertriebsmechanismus für die Patienten in Frankreich zur Verfügung ein ATU (temporäre Nutzungsberechtigung) genannt. Dieser Mechanismus ermöglicht es den Zugang der Patienten zu potenziell lebensrettende Medikamente vor der vollständigen Preis- und Erstattungs Genehmigung.
Über Iclusig ® (Ponatinibs) Tabletten
Iclusig ist ein Kinase-Inhibitor. Das primäre Ziel für Iclusig ist BCR-ABL, eine abnorme Tyrosinkinase, die bei chronischer myeloischer Leukämie (CML) und Philadelphia-Chromosom-positiver akuter lymphoblastischer Leukämie (Ph + ALL) exprimiert wird. Iclusig wurde mit ARIAD der Rechen- und strukturbasiertes Wirkstoffdesign Plattform, die speziell zur Hemmung der Aktivität von BCR-ABL entworfen. Iclusig Ziele nicht nur native BCR-ABL, sondern auch seine Isoformen, die Mutationen tragen, die Resistenz gegen die Behandlung verleihen, einschließlich der T315I-Mutation, die mit einer Resistenz gegen andere zugelassene TKI in Verbindung gebracht.
Iclusig wird in den USA, Europa, Australien, der Schweiz, Israel und Kanada zugelassen.
In den USA ist Iclusig ein Kinase-Hemmer für die angezeigte:
- Die Behandlung von erwachsenen Patienten mit T315I-positiver chronisch-myeloischer Leukämie (chronische Phase, beschleunigte Phase oder Blastenphase) oder T315I-positive Philadelphia-Chromosom-positiver akuter lymphoblastischer Leukämie (Ph + ALL).
- Die Behandlung von erwachsenen Patienten mit chronischer Phase, beschleunigte Phase oder Blastenphase chronisch-myeloischer Leukämie oder Ph + ALL, für die keine andere Tyrosinkinase-Inhibitor (TKI) Therapie indiziert ist.
Diese Angaben basieren auf Ansprechrate. Es gibt keine Studien eine Verbesserung der krankheitsbedingten Symptome oder ein verlängertes Überleben mit Iclusig überprüfen.
WICHTIGE SICHERHEITS Informationen, einschließlich der Warnung auf der Verpackung
WARNUNG: Gefäßokklusion, Herzversagen und Hepatotoxizität
Siehe vollständigen Verschreibungsinformationen für die komplette Box Warnung
Vascular Occlusion: Arterielle und venöse Thrombose und Verstopfungen in mindestens 27% traten von Iclusig Patienten behandelt, einschließlich tödlicher Myokardinfarkt, Schlaganfall, Stenose der großen arteriellen Gefäße des Gehirns, schwere periphere arterielle Verschlusskrankheit, und die Notwendigkeit für dringende Revaskularisierung Verfahren. Patienten mit und ohne kardiovaskulären Risikofaktoren, einschließlich Patienten , die jünger als 50 Jahre alt, erlebt diese Ereignisse. Überwachen Sie auf Anzeichen von Thromboembolien und Gefäßverschluss. Interrupt oder stoppen Iclusig sofort für Gefäßverschluss. Ein Nutzen - Risiko - Betrachtung sollte eine Entscheidung führen Iclusig Therapie neu zu starten.
Herzversagen, einschließlich Todesfälle traten bei 8% der Iclusig behandelten Patienten. Überwachung der Herzfunktion. Interrupt oder Iclusig für neue oder Verschlechterung der Herzinsuffizienz zu stoppen.
Hepatotoxizität, Leberversagen und Tod haben in Iclusig behandelten Patienten aufgetreten ist . Überwachung der Leberfunktion. Interrupt Iclusig wenn Hepatotoxizität vermutet wird.
Bitte beachten Sie die vollständigen US - Verschreibungsinformationen für Iclusig, einschließlich der Boxed Warning, für weitere wichtige Informationen zur Sicherheit.
In der EU Iclusig ist für die Behandlung von erwachsenen Patienten mit chronischer Phase, beschleunigte Phase oder Blastenphase chronisch-myeloischer Leukämie (CML), die gegen Dasatinib oder Nilotinib resistent sind genehmigt; die eine Unverträglichkeit gegen Dasatinib oder Nilotinib und für die nachfolgende Behandlung mit Imatinib nicht klinisch angemessen ist; oder bei denen die T315I Mutation oder die Behandlung von erwachsenen Patienten mit Philadelphia-Chromosom-positiver akuter lymphoblastischer Leukämie (Ph + ALL), die gegen Dasatinib resistent sind; die eine Unverträglichkeit gegen Dasatinib und für die nachfolgende Behandlung mit Imatinib klinisch nicht angebracht; oder die die T315I Mutation haben.
Klicken Sie hier die Iclusig EU Zusammenfassung des Arzneimittels Eigenschaften anzuzeigen. Klicke hier , um die EU - Liebe Healthcare Provider Brief (PDF) zu sehen.
Über ARIAD
ARIAD Pharmaceuticals, Inc., mit Hauptsitz in Cambridge, Massachusetts und Lausanne, Schweiz, ist ein Unternehmen für seltene Leiden Onkologie konzentriert sich auf das Leben von Krebspatienten mit Durchbruch Medikamente verwandeln. ARIAD auf neue Medikamente arbeiten, um die Behandlung verschiedener Formen von chronischen und akuten Leukämie, Lungenkrebs und andere Krebsarten Waise zu fördern. ARIAD verwendet Rechen- und strukturelle Ansätze kleinmolekularer Medikamente zu entwickeln, die Resistenz gegen vorhandene Krebsmedikamente zu überwinden. Weitere Informationen finden Sie unter http://www.ariad.com oder folgen Sie ARIAD auf Twitter ( @ARIADPharm ).
Vorausschauende Aussagen
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen, von denen jede in ihrer Gesamtheit durch diese vorbehaltlichen Aussagen qualifiziert sind. Alle hierin enthaltenen Aussagen, beschreiben keine historischen Tatsachen darstellen, einschließlich, aber nicht beschränkt auf ARIAD die Aufzeichnung der kumulativen Iclusig Einnahmen für Frankreich im zweiten Quartal 2016 begrenzt sind zukunftsgerichtete Aussagen, die auf den Erwartungen des Managements basieren und unterliegen bestimmten Faktoren, Risiken und Unsicherheiten, von denen die tatsächlichen Ergebnisse, Ergebnis der Ereignisse, den Zeitpunkt und die Leistung erheblich ausgedrückt oder impliziert durch solche Aussagen führen können. Zu diesen Faktoren, Risiken und Unsicherheiten beinhalten, sind aber nicht beschränkt auf, unsere laufenden strategischen Überprüfung, unsere Fähigkeit, erfolgreich zu vermarkten und generieren Gewinne aus dem Verkauf von Iclusig und unserer Produktkandidaten, wenn genehmigt; Konkurrenz von alternativen Therapien; unsere Fähigkeit, erwartete klinische Studie Beginn, Einschreibung und Fertigstellungstermine und die regulative Einreichung Termine für unsere Produkte und Produktkandidaten zu treffen und neue Entwicklungskandidaten in die Klinik zu bewegen; unsere Fähigkeit, auf unsere wichtigsten Unternehmensinitiativen auszuführen; regulatorische Entwicklungen und Sicherheitsfragen, einschließlich Schwierigkeiten oder Verzögerungen bei der Erlangung der behördlichen und Preis- und Erstattungs Zulassungen unserer Produkte auf den Markt; unser Vertrauen auf die Leistung von Drittherstellern und Spezial Apotheken für die Lieferung und den Vertrieb unserer Produkte und Produktkandidaten; das Auftreten ungünstiger Sicherheitsereignisse mit unseren Produkten und Produktkandidaten; die Kosten im Zusammenhang mit Forschung, Entwicklung, Herstellung, Vermarktung und andere Aktivitäten; das Verhalten, das Timing und die Ergebnisse der vorklinischen und klinischen Studien unserer Produkte und Produktkandidaten, einschließlich der präklinischen Daten und frühen klinischen Daten können später nicht mehr Phase der klinischen Studien repliziert werden; die Angemessenheit unserer Kapitalressourcen und die Verfügbarkeit von zusätzlichen Mittel; die Fähigkeit, unsere vertraglichen Verpflichtungen zu erfüllen, im Rahmen unserer Leasingverträge, Wandelanleihen und Lizenzfinanzierungsvereinbarungen einschließlich; Patentschutz und Dritter an geistigem Eigentum Ansprüche; Rechtsstreitigkeiten; unsere Aktivitäten im Ausland; Risiken in Bezug auf wichtige Mitarbeiter, Märkte, Wirtschaftsbedingungen, Gesundheitsreform, Preise und Erstattungssätze; und andere Risikofaktoren in unseren öffentlichen Einreichungen bei der US Securities and Exchange Commission detailliert, einschließlich unseres aktuellen Jahresbericht auf Formular 10-K und nachfolgenden Quartalsberichten auf Formular 10-Q. Sofern nicht anders angegeben, diese vorausschauenden Aussagen gelten nur ab dem Datum dieser Pressemitteilung und wir übernehmen keine Verpflichtung zur Aktualisierung oder eine dieser Aussagen zu revidieren, um Ereignisse oder Umstände, die nach dieser Pressemitteilung widerspiegeln. Wir warnen Investoren erhebliche Abhängigkeit von den zukunftsgerichteten Aussagen in dieser Pressemitteilung zu verlassen.
Iclusig ® ist ein eingetragenes Warenzeichen von ARIAD Pharmaceuticals, Inc.
Quelltext anzeigen Version auf businesswire.com: http://www.businesswire.com/news/home/20160519005215/en/
Kontakt:
ARIAD Pharmaceuticals, Inc.
Für Investoren
Maria Cantor, 617-621-2208
Maria.cantor@ariad.com
oder
Für Medien
Liza heapes, 617-621-2315
Liza.heapes@ariad.com
Veröffentlicht am 23. Mai 2016 von Justin Garson in Analyst Artikel - US , Investitionen
http://sleekmoney.com/...ing-reaffirmed-by-cowen-and-company/1235054/
Ariad Pharmaceuticals, Inc. (NASDAQ: ARIA) s Lager hatte seine "outperform" -Rating von Aktienanalysten bei Cowen and Company in einem Bericht bekräftigte am Donnerstag ausgegeben. Sie verfügen derzeit über einen 10,00 $ Kursziel für die Pharma-Aktien des Unternehmens. Cowen and Company Kursziel zeigt ein Aufwärtspotenzial von 29,03% gegenüber dem aktuellen Aktienkurs.
Mehrere große Investoren geändert kürzlich ihre Bestände an ARIA. Dekabank Deutsche Girozentrale steigerte seinen Anteil an Aktien von Ariad Pharmaceuticals um 1,1% im vierten Quartal. Die Dekabank Deutsche Girozentrale besitzt nun 96.000 Aktien der Aktie bei $ 609.000 geschätzt Pharmaunternehmen nach dem in der Zeit weitere 1.000 Kauf von Aktien. Retirement System California State Teachers steigerte ihren Anteil an der Ariad Pharmaceuticals um 1,6% im vierten Quartal. California State Teachers Retirement System besitzt nun 310.276 Aktien der Aktie bei $ 1.939.000 geschätzt Pharmaunternehmen nach weitere 5.000 Aktien im letzten Quartal zu kaufen. Rhumbline Berater verstärkt ihre Beteiligung an der Ariad Pharmaceuticals um 7,8% im vierten Quartal. Rhumbline Advisers besitzt nun 174.193 Aktien der Aktie bei $ 1.089.000 geschätzt Pharmaunternehmen nach einer zusätzlichen 12.560 Aktien im letzten Quartal zu kaufen. Asset Management Oxford steigerte ihren Anteil an der Ariad Pharmaceuticals um 60,9% im vierten Quartal. Oxford Asset Management besitzt nun 476.178 Aktien der Aktie bei $ 3.012.000 geschätzt Pharmaunternehmen nach einer zusätzlichen 180.186 Aktien im letzten Quartal zu kaufen. Schließlich steigerte ProShare Advisors LLC ihre Beteiligung an der Ariad Pharmaceuticals um 10,3% im vierten Quartal. ProShare Advisors LLC besitzt nun 176.600 Aktien der Aktie bei $ 1.104.000 geschätzt Pharmaunternehmen nach einer zusätzlichen 16.552 Aktien im letzten Quartal zu kaufen.
In Verbindung stehende News, verkauft VP Daniel M. Bollag 9625 Aktien der Aktien der Unternehmen im Rahmen einer Transaktion, die am Donnerstag stattgefunden, 3. März. Die Aktien wurden zu einem durchschnittlichen Preis von $ 6.11 für einen Gesamtwert von $ 58,808.75 verkauft. Nach dem Abschluss des Verkaufs, besitzt der Vizepräsident jetzt direkt 160.713 Aktien der Gesellschaft im Wert von $ 981,956.43. Der Verkauf wurde in einer Einreichung bei der SEC offenbart, die an verfügbar ist diesem Link . Auch verkauft VP Edward M. Fitzgerald 5417 Aktien der Aktien der Unternehmen im Rahmen einer Transaktion, die am Montag, 21. MÄRZ aufgetreten. Die Aktien wurden zu einem durchschnittlichen Preis von $ 6,47 für einen Gesamtwert von $ 35,047.99 verkauft. Nach dem Abschluss des Verkaufs, besitzt der Vizepräsident jetzt 325.784 Aktien der Aktien des Unternehmens, bei 2,107,822.48 $ geschätzt. Die Offenbarung für diesen Verkauf kann gefunden werden hier .
Andere Aktien-Analysten auch Forschungsberichte über das Unternehmen vor kurzem ausgestellt. Goldman Sachs senkte ihr Kursziel auf Ariad Pharmaceuticals von $ 7,00 bis $ 5,00 in einem Forschungsbericht am Montag 22. Februar. Zacks Investment Research stufte Ariad Pharmaceuticals von einem "buy" -Rating mit einem Rating "halten" in einem Forschungsbericht am Dienstag 26. April. RBC Capital neu aufgelegt eine Rating "halten" auf Aktien von Ariad Pharmaceuticals in einem Forschungsbericht am Donnerstag, 25. Februar. JPMorgan Chase & Co. verstärkt ihr Kursziel auf Ariad Pharmaceuticals von $ 9,00 bis $ 11,00 und gab die Aktie einen "Markt outperform" -Rating in einem Forschungsbericht am Mittwoch, 9. MÄRZ. Schließlich senkte JMP Securities ihr Kursziel auf Ariad Pharmaceuticals von $ 11,00 bis $ 9,00 und legen Sie einen "Markt outperform" -Rating für die Aktie in einem Forschungsbericht am Mittwoch, 9. März. Zwei Analysten haben die Aktie mit einer Verkaufs bewertet, zwei eine Halte Bewertung abgegeben haben, fünf haben eine Kaufempfehlung zugewiesen und hat man eine starke Kaufempfehlung für das Unternehmen zugeordnet. Die Aktie hat derzeit einen Konsens-Rating von "Buy" und einem durchschnittlichen Kursziel von $ 8,71.
Ariad Pharmaceuticals (NASDAQ: ARIA) eröffnet bei 7,75 am Donnerstag. Die Marktkapitalisierung des Unternehmens $ 1480000000. Ariad Pharmaceuticals verfügt über eine 52-Wochentief von 4,37 $ und eine 52-Wochenhoch von 10,07 $. Die Firma 50-Tage gleitenden Durchschnittspreis ist 7,08 $ und seine 200-Tage-Durchschnittspreis beträgt $ 6.25.
Ariad Pharmaceuticals (NASDAQ: ARIA) freigegeben zuletzt das Ergebnis Ergebnisse am Dienstag, 10. MAI. Das Pharmaunternehmen berichtet ($ 0,23) Ergebnis je Aktie (EPS) für das Quartal, von Analysten Konsensschätzungen von ($ 0,27) zu schlagen $ 0,04. Das Unternehmen verdiente $ 35,60 Millionen im Quartal, im Vergleich zu Analystenschätzungen von $ 43.060.000. Während des gleichen Zeitraums im Vorjahr erzielte die Firma ($ 0,28) EPS. Ariad Pharmaceuticals Der Umsatz stieg um 48,3% im Vergleich zum gleichen Quartal des Vorjahres. Im Durchschnitt Aktien-Analysten prognostizieren, dass Ariad Pharmaceuticals ($ 0,59) EPS für das laufende Geschäftsjahr wird Post.
ARIAD Pharmaceuticals, Inc. ist ein globales Onkologie-Unternehmen. Die Gesellschaft ist in der Entdeckung, Entwicklung und Vermarktung von niedermolekularen Wirkstoff für die Behandlung von Krebs angezeigt engagiert. Die Produktpipeline des Unternehmens umfasst Iclusig (Ponatinibs), brigatinib (AP26113), AP32788 und ridaforolimus.
Date : 05/24/2016 @ 9:25AM
Source : Business Wire
Stock : Ariad Pharmaceuticals, Inc. (MM) (ARIA)
Quote : 7.98 -0.1 (-1.24%) @ 3:56PM
http://ih.advfn.com/p.php?pid=nmona&article=71561432
ARIAD Pharmaceuticals, Inc. (Nasdaq: ARIA) kündigte die Einleitung der Phase 1/2 der klinischen Prüfung AP32788, ein Prüfpräparat Tyrosinkinase-Inhibitor (TKI), die als eine zielgerichtete Therapie für Patienten mit nicht-kleinzelligem Lungenkrebs (NSCLC) mit spezifischen Mutationen in EGFR oder HER2. AP32788 Ziele Tumoren von EGFR oder HER2-Kinasen angetrieben und wurde selektive Hemmung dieser Kinasen mit Exon 20 Mutationen zu erreichen. Es gibt derzeit keine zugelassenen gezielte Behandlungsmöglichkeiten zur Verfügung für die etwa vier bis neun Prozent der EGFR-mutierten Tumoren der Lunge mit Exon 20 Insertionsmutationen in NSCLC patients.1 Zusätzlich etwa zwei Prozent der NSCLC Patienten2 haben HER2 Mutationen, mit der Mehrheit Exon 20 Insertionsmutationen.
"In den präklinischen Daten auf der AACR Sitzung im vergangenen Monat vorgestellt, AP32788 die Fähigkeit bewiesen alle getesteten EGFR und HER2-Mutanten zu hemmen, einschließlich Exon 20 Insertionsmutanten", erklärte Tim Clackson, Ph.D., President für Forschung und Entwicklung und der wissenschaftlichen Leiter Officer von ARIAD. "Wir freuen uns, AP32788 vorantreiben, um die nächste viel versprechende Krebsmedizin in der ARIAD Pipeline in die klinische Studie für Patienten, die derzeit keine gezielten Therapiemöglichkeiten in dieser Orphan-Onkologie Krankheit Untergruppen haben."
Clinical Trial Design-
Die Studie wird in zwei Teilen durchgeführt werden: eine Dosiseskalationsphase, gefolgt von einer Expansionsphase. Die erste Phase-1-Dosis-Eskalationsstudie Segment Patienten mit fortgeschrittenem NSCLC sind. Die Patienten in dieser multizentrischen Studie aufgenommen werden, um Standard verfügbaren Therapien feuerfeste sein. Das primäre Ziel der Phase-1-Segment der Studie ist die Sicherheit, Verträglichkeit, pharmakokinetische Profil und die empfohlenen Phase-2-Dosis (RP2D) von oral verabreichtem AP32788 zu bestimmen. ARIAD erwartet in diesem Teil der Studie etwa 20 bis 30 Patienten einzuschreiben.
Die Phase-2-Expansionsphase der Studie werden vier histologisch und molekular definierte Patientengruppen umfassen, einschließlich:
NSCLC-Patienten mit EGFR Exon 20 Einfügungen ohne aktive, messbare zentrale Nervensystem zu aktivieren (ZNS) Metastasen;
NSCLC-Patienten mit HER2-Exon 20 Einfügungen oder Punktmutationen ohne aktive, messbare ZNS-Metastasen zu aktivieren;
NSCLC-Patienten mit EGFR Exon 20 aktivierenden Einfügungen oder HER2 Exon 20 Einfügungen oder Punktmutationen und aktiv, messbare ZNS-Metastasen zu aktivieren; und,
NSCLC mit anderen Ziele, gegen die hat AP32788 präklinische Aktivität gezeigt (Beispiele umfassen EGFR Exon 19 Deletionen oder Exon 21 Substitutionen [mit oder ohne T790M Mutationen] und andere seltene aktivierende EGFR-Mutationen) mit oder ohne aktive, messbare ZNS-Metastasen.
Die Phase-2-Segment der Studie ist geplant, rund 80 Patienten einschreiben und Anti-Tumor-Aktivität von AP32788 in dieser molekular definierten Patientenpopulationen zu bewerten.
CAMBRIDGE, Mass.--(BUSINESS WIRE)--Jun. 1, 2016-- ARIAD Pharmaceuticals, Inc. (NASDAQ: ARIA) today announced that it will present at the Jefferies 2016 Global Healthcare Conference being held in New York City. Paris Panayiotopoulos, president and chief executive officer, will provide an overview of the Company’s business on Wednesday, June 8, 2016 at 11:00 a.m. (ET).
http://investor.ariad.com/...22&p=irol-newsArticle&ID=2173858
und der Firmensitz ist in der Schweiz !!!
http://www.finanzen.ch/aktien/Ariad_Pharmaceuticals-Aktie/SWX
To Our Stockholders:
I am pleased to invite you to attend our 2016 annual meeting of stockholders, which will be held on Thursday, July 21, 2016, beginning at 10:00 a.m. EDT, at our corporate offices in Cambridge, Massachusetts.
http://ih.advfn.com/p.php?pid=nmona&article=71687225
CAMBRIDGE, Mass.--(BUSINESS WIRE)--Jun. 8, 2016-- ARIAD Pharmaceuticals, Inc. (NASDAQ: ARIA) today announced that it will host an Analyst & Investor Day for its research analysts and institutional investors on Friday, June 17 at 8:30 a.m. (EDT) in New York City. Paris Panayiotopoulos, president and chief executive officer of ARIAD, will host the event along with other key members of ARIAD senior management. The meeting will focus on ARIAD’s completion of its corporate strategic review, as well as provide an update on continued progress in its research and development and commercial programs. Expert medical leaders in the fields of chronic myeloid leukemia and non-small cell lung cancer will be featured speakers and discussants at the meeting.
http://investor.ariad.com/...;p=irol-EventDetails&EventId=5229747
13. Juni 2016, 07.39.00 EDT von RTT
http://www.nasdaq.com/article/...2-pace-clinical-trial-20160613-00196
RTTNews.com) - ARIAD Pharmaceuticals Inc. ( ARIA ) gab bekannt , Langzeit - Follow-up - Daten aus der zulassungsrelevanten Phase - 2 PACE - Studie mit Iclusig oder Ponatinib, dessen genehmigt BCR-ABL - Inhibitor, in stark vorbehandelten Patienten mit resistenten oder intoleranten chronischen myeloische Leukämie oder CML oder Philadelphia-Chromosom-positiver akuter lymphoblastischer Leukämie (Ph + ALL).
Antworten wurden langfristige in der chronischen Phase der CML (CP-CML) Patienten erhalten. Die Studie zeigt, dass mit Iclusig behandelten Patienten weiterhin mit einem medianen Follow-up von 4,0 Jahren bei CP-CML anti-leukämische Aktivität zu demonstrieren. Darüber hinaus 96 Prozent der CP-CML-Patienten, die Ponatinibs Dosisreduktionen während in Reaktion unterzog ihre Antworten beibehalten (MCyR) am 4 Jahre Zeitpunkt.
"Wir sind weiterhin sehr zufrieden mit diesen fort Antworten in der PACE-Studie in einem so stark vorbehandelten Patientenpopulation, als 59 Prozent der Patienten, die zuvor erhalten hatten drei oder mehr genehmigt Tyrosinkinase-Inhibitoren (TKI). Insgesamt 82 Prozent der CP-CML-Patienten, die erreicht MCyR geschätzt in MCyR nach vier Jahren zu bleiben ", erklärte Jorge E. Cortes
, MD, Professor und stellvertretender Vorsitzender, Abteilung für Leukämie, University of Texas MD Anderson Cancer Center.
http://www.rttnews.com
Tue, Jun 21, 2016, 6:11 AM EDT - U.S. Markets open in 3 hrs 19 mins
http://finance.yahoo.com/news/...on-agreements-iclusig-114500981.html
~ ARIAD für den Empfang von mehr als 50 Prozent von Iclusig Umsatz in diesen Regionen
~ Verträge enthalten Buy-Back Bestimmungen für den Fall eines Kontrollwechsels von ARIAD
CAMBRIDGE, Mass .-- (BUSINESS WIRE) -
ARIAD Pharmaceuticals, Inc. (ARIAD; NASDAQ: ARIA) gab heute bekannt , dass es zwei Vertriebsvereinbarungen für Iclusig Abschluss ® (Ponatinibs) , die außerhalb der Vereinigten Staaten. In Lateinamerika, ARIAD und Pint Pharma International SA, ein Unternehmen auf innovative Behandlungen für Patienten in Lateinamerika konzentriert mit Krebs, seltene Krankheiten und genetischen Störungen, haben eine Vereinbarung getroffen, für Pint Pharma Iclusig in Argentinien, Brasilien, Chile zu kommerzialisieren, Kolumbien und Mexiko. ARIAD hat sich auch in einer separaten Vereinbarung mit Biologix FZCo eingetragen., Ein führender Distributor von Spezialpharmazeutika im Nahen Osten, für Biologix Iclusig im Nahen Osten und Nordafrika (MENA), auch in Saudi-Arabien, die Golfküste Länder zu vermarkten , dem Libanon und anderen Ländern in der Region ausgewählt.
"Unsere neue Vertriebsvereinbarungen für Lateinamerika und dem Nahen Osten und Nordafrika Märkte zeigen unser Engagement Iclusig für Patienten auf der ganzen Welt zu bringen, die in Not dieser wichtigen Medizin für refraktäre CML und Ph + ALL, während sie weiterhin unsere kommerziellen Ressourcen darauf zu konzentrieren, der US-Markt ", erklärte Hugh Cole, Chief Business Officer von ARIAD. "Wir glauben, dass unsere neuen Partner in diesen Regionen haben die lokale Expertise und das Engagement, um erfolgreich Iclusig in ihren Märkten zu vermarkten. Darüber hinaus einen bedeutenden Anteil der Einnahmen aus diesen Regionen zu bieten, damit die Vereinbarungen zukünftige strategische Optionalität für ARIAD durch Rückstellungen für den Rückkauf dieser Iclusig Rechte durch einen Erwerber von ARIAD im Falle eines Kontrollwechsels von ARIAD einschließlich. "
Abkommen mit Pint Pharma
Pint Pharma hat exklusive Rechte erhalten Iclusig nach Zulassung in Argentinien, Brasilien, Chile, Kolumbien und Mexiko (das "Gebiet"), mit dem Potenzial der Zugabe von anderen lateinamerikanischen Ländern in der Zukunft zu vermarkten. ARIAD und Pint haben vereinbart, zusammenzuarbeiten Zulassungsgenehmigungen in den Ländern im Gebiet vorzulegen. Darüber hinaus hat Pint vereinbart Iclusig als Prüfpräparat auf patientenspezifischer Basis in bestimmten Ländern auf dem Gebiet zu vertreiben, in denen vor der behördlichen Genehmigung gestattet.
Im Gegenzug für diese Rechte, wird ARIAD erhalten im Voraus und mögliche regulatorische Meilensteinzahlungen in Höhe von insgesamt $ 15.000.000. ARIAD wird auch mehr als 50 Prozent des Nettoproduktverkäufe im Gebiet durch ein Produkt zu liefern Transferpreis erhalten.
"In den letzten paar Jahren haben wir auf zu bringen wichtige Onkologie und Behandlung seltener Krankheiten zu lateinamerikanischen Ländern konzentriert haben", sagte David Muñoz, Chief Executive Officer von Pint Pharma. "Gemeinsam mit ARIAD planen wir, regulatorischen und Erstattung Genehmigungen zu sichern arbeiten für Iclusig refraktär Philadelphia-positive Leukämie-Patienten in der Notwendigkeit neuer Behandlungsmöglichkeiten in dem Gebiet zur Verfügung stehen."
Die Bedingungen der Vertriebsvereinbarung enthalten eine Option für einen Käufer von ARIAD auf, indem sie bestimmte Zahlungen die Rechte an Iclusig im Gebiet folgenden drei Jahren ab dem Datum des Inkrafttretens der Vertriebsvereinbarung Rückkauf.
Abkommen mit Biologix FZCo.
Biologix hat exklusive Rechte erhalten Iclusig in Bahrain, das Königreich Saudi-Arabien, Kuwait, Oman, Katar, die Vereinigten Arabischen Emirate, im Libanon und anderen Ländern in der Region zu vermarkten. In der Anfangsphase der Vereinbarung hat Biologix vereinbart Iclusig als Prüfpräparat auf patientenspezifischer Basis in bestimmten Ländern auf dem Gebiet zu vertreiben, in denen vor der behördlichen Genehmigung erlaubt und danach Iclusig in jenen Ländern, in denen die Zulassung erreicht zu kommerzialisieren wird .
"Wir haben eine etablierte Onkologie und Hämatologie-Portfolios mit langjähriger Erfahrung im Nahen Osten, Golfküste und Nordafrika", sagte Selim Ghorayeb, Chief Executive Officer von Biologix. "Mit Blick auf unsere Partnerschaft mit ARIAD, sind wir gewidmet, diese Erfahrung zu bringen geeigneten Patienten Iclusig zu helfen, Zugang für resistente Formen der CML und Ph + ALL."
Gemäß den Bedingungen der Vertriebsvereinbarung wird ARIAD mehr als 50 Prozent des Nettoproduktumsätze im Gebiet durch ein Transferpreis Produkt zu liefern. Die Vereinbarung umfasst auch eine Option für einen Käufer von ARIAD auf, indem sie bestimmte Zahlungen die Rechte an Iclusig im Gebiet folgenden drei Jahren ab dem Datum des Inkrafttretens der Vertriebsvereinbarung Rückkauf.
Über CML und Ph + ALL
CML ist durch eine übermäßige und unregulierte Produktion von weißen Blutkörperchen im Knochenmark aufgrund einer genetischen Abnormalität gekennzeichnet, dass die BCR-ABL-Protein produziert. Nach einer chronischen Phase der Produktion von zu viele weiße Blutkörperchen, CML entwickelt typischerweise zu den aggressiveren Phasen als beschleunigte Phase und Blastenkrise bezeichnet. Ph + ALL ist ein Subtyp der akuten lymphatischen Leukämie, die die Ph + Chromosom trägt die BCR-ABL produziert. Es hat einen aggressiveren Verlauf als CML und wird oft mit einer Kombination aus Chemotherapie und Tyrosinkinase-Inhibitoren behandelt. Das BCR-ABL-Protein wird in beiden dieser Erkrankungen exprimiert.
Über Iclusig ® (Ponatinibs) Tabletten
Iclusig ist ein Kinase-Inhibitor. Das primäre Ziel für Iclusig ist BCR-ABL, eine abnorme Tyrosinkinase, die bei chronischer myeloischer Leukämie (CML) und Philadelphia-Chromosom-positiver akuter lymphoblastischer Leukämie (Ph + ALL) exprimiert wird. Iclusig wurde mit ARIAD der Rechen- und strukturbasiertes Wirkstoffdesign Plattform, die speziell zur Hemmung der Aktivität von BCR-ABL entworfen. Iclusig Ziele nicht nur native BCR-ABL, sondern auch seine Isoformen, die Mutationen tragen, die Resistenz gegen die Behandlung verleihen, einschließlich der T315I-Mutation, die mit einer Resistenz gegen andere zugelassene TKI in Verbindung gebracht.
Iclusig wird in den USA, Europa, Australien, der Schweiz, Israel und Kanada zugelassen.
In den USA ist Iclusig ein Kinase-Hemmer für die angezeigte:
• Behandlung von erwachsenen Patienten mit T315I-positiver chronisch-myeloischer Leukämie (chronische Phase, beschleunigte Phase oder Blastenphase) oder T315I-positive Philadelphia-Chromosom-positiver akuter lymphoblastischer Leukämie (Ph + ALL).
• Behandlung von erwachsenen Patienten mit chronischer Phase, beschleunigte Phase oder Blastenphase chronisch-myeloischer Leukämie oder Ph + ALL, für die keine andere Tyrosinkinase-Inhibitor (TKI) Therapie indiziert ist.
Diese Angaben basieren auf Ansprechrate. Es gibt keine Studien eine Verbesserung der krankheitsbedingten Symptome oder ein verlängertes Überleben mit Iclusig überprüfen.
Nutzungsbeschränkungen:
Iclusig wird nicht angezeigt und ist nicht für die Behandlung von Patienten mit neu diagnostizierter CML im chronischen Stadium empfohlen
WICHTIGE SICHERHEITS Informationen, einschließlich der Warnung auf der Verpackung
WARNUNG: Gefäßokklusion, Herzversagen und Hepatotoxizität
Siehe vollständigen Verschreibungsinformationen für die komplette Box Warnung
Vascular Occlusion •: Arterielle und venöse Thrombose und Verstopfungen in mindestens 27% traten von Iclusig Patienten behandelt, einschließlich tödlicher Myokardinfarkt, Schlaganfall, Stenose der großen arteriellen Gefäße des Gehirns, schwere periphere arterielle Verschlusskrankheit, und die dringende Notwendigkeit von Revaskularisierungsverfahren . Patienten mit und ohne kardiovaskulären Risikofaktoren, einschließlich Patienten , die jünger als 50 Jahre alt, erlebt diese Ereignisse. Überwachen Sie auf Anzeichen von Thromboembolien und Gefäßverschluss. Interrupt oder stoppen Iclusig sofort für Gefäßverschluss. Ein Nutzen - Risiko - Betrachtung sollte eine Entscheidung führen Iclusig Therapie neu zu starten.
• Herzversagen, einschließlich Todesfälle traten bei 8% der Iclusig behandelten Patienten. Überwachung der Herzfunktion. Interrupt oder Iclusig für neue oder Verschlechterung der Herzinsuffizienz zu stoppen.
• Hepatotoxizität, Leberversagen und Tod haben in Iclusig behandelten Patienten aufgetreten ist . Überwachung der Leberfunktion. Interrupt Iclusig wenn Hepatotoxizität vermutet wird.
Bitte beachten Sie die vollständigen US - Verschreibungsinformationen für Iclusig, einschließlich der Boxed Warning, für weitere wichtige Informationen zur Sicherheit.
Über ARIAD
ARIAD Pharmaceuticals, Inc., mit Hauptsitz in Cambridge, Massachusetts wird sich auf die Entdeckung, Entwicklung und Vermarktung von Präzisions Therapien für Patienten mit seltenen Krebserkrankungen. ARIAD auf neue Medikamente arbeiten, um die Behandlung von seltenen Formen der chronischen und akuten Leukämie, Lungenkrebs und andere seltene Krebserkrankungen voranzubringen. ARIAD verwendet Rechen- und strukturelle Ansätze kleinmolekularer Medikamente zu entwickeln, die Resistenz gegen vorhandene Krebsmedikamente zu überwinden. Weitere Informationen finden Sie unter http://www.ariad.com oder folgen Sie ARIAD auf Twitter (@ARIADPharm).
Über Pint Pharma
Pint Pharma ist ein privates Unternehmen für Spezialpharmaka, die im Pharmasektor von spezialisierten Führern mit umfangreicher Erfahrung zugute kommt und wem basieren strategisch in ganz Lateinamerika und Europa. Pint Pharma hat auch eine lange Erfolgsbilanz bei der Entwicklung von starken Beziehungen mit weltweit tätigen Pharma- und Healthcare-Unternehmen. Pint Pharma hat den Ehrgeiz, ein führender lateinamerikanischen Unternehmen liefert innovative Behandlungen für Patienten mit Krebs, seltene Krankheiten und genetische Erkrankungen zu werden.
Über Biologix FZCo.
Biologix FZCo. befindet sich in der Dubai Airport Free Zone als regionale Förderer des Spezialpharma-Produkte integriert. Biologix konzentriert sich auf die Onkologie-Hämatologie, Kardiologie, zentrales Nervensystem, und seltene Krankheiten.
Biologix FZCo. Mission ist es, die Verfügbarkeit in den MENA-Märkten von innovativen Therapien zu beschleunigen, die normalerweise erst viel später durch den Fokus ihrer Hersteller auf den größeren Märkten in Nordamerika, Europa und Japan zur Verfügung stehen würden. Biologix ermöglicht eine Win-Win-Ergebnis für Patienten, die auf eine wirksame Behandlung vermissen würde und für die Hersteller, die nicht die MENA-Märkte in einem so frühen Stadium ihrer Unternehmensentwicklung zugreifen würde.
ARIAD Zukunftsgerichtete Aussagen
Diese Pressemitteilung enthält zukunftsgerichtete Aussagen, von denen jede in ihrer Gesamtheit durch diese vorbehaltlichen Aussagen qualifiziert sind. Alle hierin enthaltenen Aussagen, beschreiben keine historischen Tatsachen darstellen, einschließlich, aber nicht beschränkt auf, die Fähigkeit von Pint Pharma und Biologix FZCo. (Zusammen die "Vertriebsstellen"), um die vertraglich vereinbarten Leistungen zu erbringen, wie zum Beispiel den Erhalt der behördlichen Genehmigungen für Iclusig in ihren jeweiligen Gebieten; Die Vertriebsstellen die Fähigkeit, zu fördern, vermarkten und verkaufen Iclusig in ihren jeweiligen Gebieten zu verteilen; der Zeitpunkt und Umfang der behördlichen Genehmigungen in den abgedeckten Gebieten erhalten; das Timing und der Erfolg der Verkäufe von Iclusig in den Gebieten; und die Aussagen von den Beamten von ARIAD, Pint Pharma und Biologix FZCo., sind zukunftsgerichtete Aussagen, die auf den Erwartungen des Managements basieren und unterliegen bestimmten Faktoren, Risiken und Unsicherheiten, welche die tatsächlichen Ergebnisse, die Ergebnisse der Ereignisse, Timing verursachen und Leistung erheblich von jenen unterscheiden in diesen Aussagen ausgedrückt oder impliziert werden. Zu diesen Faktoren, Risiken und Unsicherheiten beinhalten, sind aber nicht beschränkt auf, die Konkurrenz durch alternative Therapien; regulatorische Entwicklungen und Sicherheitsfragen, einschließlich Schwierigkeiten oder Verzögerungen bei der Erlangung der behördlichen und Preis- und Erstattungs Zulassungen unserer Produkte auf den Markt; unser Vertrauen auf die Leistung von Drittherstellern und Spezial Apotheken für die Lieferung und den Vertrieb unserer Produkte und Produktkandidaten; das Auftreten ungünstiger Sicherheitsereignisse mit unseren Produkten und Produktkandidaten; die Kosten im Zusammenhang mit Forschung, Entwicklung, Herstellung, Vermarktung und andere Aktivitäten; die Angemessenheit unserer Kapitalressourcen und die Verfügbarkeit von zusätzlichen Mittel; unsere Aktivitäten im Ausland; Risiken in Bezug auf wichtige Mitarbeiter, Märkte, Wirtschaftsbedingungen, Gesundheitsreform, Preise und Erstattungssätze; und andere Risikofaktoren in unseren öffentlichen Einreichungen bei der US Securities and Exchange Commission detailliert, einschließlich unseres aktuellen Jahresbericht auf Formular 10-K und nachfolgenden Quartalsberichten auf Formular 10-Q. Sofern nicht anders angegeben, diese vorausschauenden Aussagen gelten nur ab dem Datum dieser Pressemitteilung und wir übernehmen keine Verpflichtung zur Aktualisierung oder eine dieser Aussagen zu revidieren, um Ereignisse oder Umstände, die nach dieser Pressemitteilung widerspiegeln. Wir warnen Investoren erhebliche Abhängigkeit von den zukunftsgerichteten Aussagen in dieser Pressemitteilung zu verlassen.
Quelltext anzeigen Version auf businesswire.com: http://www.businesswire.com/news/home/20160617005266/en/
Kontakt:
ARIAD Pharmaceuticals, Inc.
Investoren
Manmeet S. Soni, 617-503-7298
Manmeet.soni@ariad.com
oder
Medien
Liza heapes, 617-621-2315
Liza.heapes@ariad.com